- 1 Визначення хвороби. Причини захворювання
- 2 Симптоми тромбоемболії легеневої артерії
- 3 Патогенез тромбоемболії легеневої артерії
- 4 Класифікація та стадії розвитку тромбоемболії легеневої артерії
- 5 Ускладнення тромбоемболії легеневої артерії
- 6 Діагностика тромбоемболії легеневої артерії
- 7 Лікування тромбоемболії легеневої артерії
- 8 Прогноз. Профілактика
Що таке тромбоемболія легеневої артерії? Причини виникнення, діагностику та методи лікування розберемо в статті.
Визначення хвороби. Причини захворювання
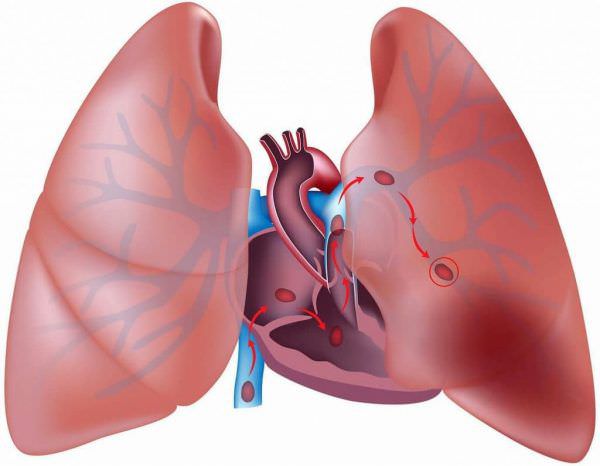
Тромбоемболія легеневої артерії (ТЕЛА) – закупорка артерій малого кола кровообігу кров’яними згустками, що утворилися в венах великого кола кровообігу і правих відділах серця, принесеними з потоком крові. В результаті чого припиняється кровопостачання легеневої тканини, розвивається некроз (відмирання тканин), виникає інфаркт-пневмонія, дихальна недостатність. Збільшується навантаження на праві відділи серця, розвивається правошлуночкова недостатність кровообігу: ціаноз (посиніння шкіри), набряки на нижніх кінцівках, асцит (скупчення рідини в черевній порожнині). Захворювання може розвиватися гостро або поступово, протягом декількох годин або днів. У важких випадках розвиток ТЕЛА відбувається стрімко і може призвести до різкого погіршення стану і загибелі хворого.
Щороку від ТЕЛА помирає 0,1% населення земної кулі. За частотою смертей захворювання поступається лише ІХС (ішемічна хвороба серця) та інсульту. Хворих ТЕЛА помирає більше, ніж хворих на СНІД, рак молочної, передміхурової залоз та постраждалих в дорожньо-транспортних пригодах разом узятих. Більшості хворим (90%), померлим від ТЕЛА, вчасно не був встановлений правильний діагноз, і не було проведено необхідне лікування. ТЕЛА часто виникає там, де її не очікують – у хворих некардіологічними захворюваннями (травми, пологи), ускладнюючи їх перебіг. Смертність при ТЕЛА досягає 30%. При своєчасному оптимальному лікуванні смертність може бути знижена до 2-8%.
Прояв захворювання залежить від величини тромбів, раптовості або поступовості появи симптомів, тривалості захворювання. Перебіг може бути дуже різним – від безсимптомного до швидкопрогресуючого, аж до раптової смерті.
Тромбоемболія легеневої артерії – хвороба-привид, яка носить маски інших захворювань серця або легенів. Клініка може бути інфарктоподібна, нагадувати бронхіальну астму, гостру пневмонію. Іноді першим проявом хвороби є правошлуночкова недостатність кровообігу. Головна відмінність – раптовий початок за відсутності інших видимих причин наростання задишки.
ТЕЛА розвивається, як правило, в результаті тромбозу глибоких вен, який передує зазвичай за 3-5 днів до початку захворювання, особливо при відсутності антикоагулянтної терапії.
Фактори ризику тромбоемболії легеневої артерії
При діагностиці враховують наявність факторів ризику тромбоемболії. Найбільш значимі з них: перелом шийки стегна або кінцівки, протезування стегнового або колінного суглоба, велика операція, травма або ураження мозку.
До небезпечних (але не настільки сильно) чинників відносять: артроскопію колінного суглоба, центральний венозний катетер, хіміотерапію, хронічну серцеву недостатність, гормонозамінну терапію, злоякісні пухлини, оральні контрацептиви, інсульт, вагітність, пологи, післяпологовий період, тромбофілія. При злоякісних новоутвореннях частота венозної тромбоемболії становить 15% і є другою за значимістю причиною смерті цієї групи хворих. Хіміотерапевтичне лікування збільшує ризик венозної тромбоемболії на 47%. Нічим не спровокована венозна тромбоемболія може бути раннім проявом злоякісного новоутворення, яке діагностується протягом року у 10% пацієнтів епізоду ТЕЛА.
До найбільш безпечних, але все ж маючих ризик, чинників відносять всі стани, пов’язані з тривалою іммобілізацією (нерухомістю) – тривалий (більше трьох діб) постільний режим, авіаперельоти, похилий вік, варикозне розширення вен, лапароскопічні втручання.
Деякі фактори ризику – спільні з тромбозами артеріального русла. Це ті ж фактори ризику ускладнень атеросклерозу і гіпертонічної хвороби: куріння, ожиріння, малорухливий спосіб життя, а також цукровий діабет, гіперхолестеринемія, психологічний стрес, низький рівень вживання овочів, фруктів, риби, низький рівень фізичної активності.
Чим більше вік хворого, тим більше вірогідний розвиток захворювання.
Нарешті, сьогодні доведено існування генетичної схильності до ТЕЛА. Гетерозиготна форма поліморфізму V фактора збільшує ризик вихідних венозних тромбоемболій в три рази, а гомозиготна форма – в 15-20 разів.
До найбільш значущих чинників ризику, що сприяють розвитку агресивної тромбофілії, відносяться антифосфоліпідний синдром з підвищенням антикардіоліпінових антитіл і дефіцит природних антикоагулянтів: протеїну С, протеїну S і антитромбіну III.
Симптоми тромбоемболії легеневої артерії
Симптоми захворювання різноманітні. Не існує жодного симптому, при наявності якого можна було точно сказати, що у хворого виникла ТЕЛА.
При тромбоемболії легеневої артерії можуть зустрічатися загрудинні інфарктоподібні болі, задишка, кашель, кровохаркання, артеріальна гіпотонія, ціаноз, синкопальні стани (непритомність), що також може зустрічатися і при інших різних захворюваннях.
Часто діагноз ставиться після виключення гострого інфаркту міокарда. Характерною особливістю задишки при ТЕЛА є виникнення її без зв’язку із зовнішніми причинами. Наприклад, хворий відзначає, що не може піднятися на другий поверх, хоча напередодні робив це без зусиль. При ураженні дрібних гілок легеневої артерії симптоматика на самому початку може бути стертою, неспецифічної. Лише на 3-5 день з’являються ознаки інфаркту легені: болі в грудній клітці; кашель; кровохаркання; поява плеврального випоту (скупчення рідини у внутрішній порожнині тіла). Гарячковий синдром спостерігається в період від 2 до 12 днів.
Повний комплекс симптомів зустрічається лише у кожного сьомого хворого, проте 1-2 ознаки зустрічаються у всіх пацієнтів. При ураженні дрібних гілок легеневої артерії діагноз, як правило, виставляється лише на етапі виникнення інфаркту легені, тобто через 3-5 доби. Іноді хворі з хронічною ТЕЛА тривалий час спостерігаються у пульмонолога, в той час як своєчасна діагностика і лікування дозволяють зменшити задишку, поліпшити якість життя і прогноз.
Тому з метою мінімізації витрат на діагностику розроблені шкали для визначення ймовірності захворювання. Ці шкали вважаються практично рівноцінними, але Женевська модель виявилася більш прийнятною для амбулаторних пацієнтів, а шкала PSWells – для стаціонарних. Вони дуже прості у використанні, включають в себе як основні причини (тромбоз глибоких вен, новоутворення в анамнезі), так і клінічні симптоми.
Паралельно з діагностикою ТЕЛА лікар повинен визначити джерело тромбозу, і це досить важке завдання, так як утворення тромбів у венах нижніх кінцівок часто протікає безсимптомно.
Патогенез тромбоемболії легеневої артерії
В основі патогенезу лежить механізм венозного тромбозу. Тромби в венах утворюються внаслідок зниження швидкості венозного кровотоку через виключення пасивного скорочення венозної стінки при відсутності м’язових скорочень, варикозному розширенні вен, здавленні їх об’ємними утвореннями. На сьогоднішній день лікарі не можуть поставити діагноз розширення вен малого тазу (у 40% хворих). Венозний тромбоз може розвиватися при:
- порушенні згортання крові – патологічних або ятрогенних (одержаному в результаті лікування, а саме при прийомі ГПЗТ);
- пошкодженні судинної стінки внаслідок травм, оперативних втручань, тромбофлебіту, ураження її вірусами, вільними радикалами при гіпоксії, отрутами.
Тромби можуть бути виявлені за допомогою ультразвуку. Небезпечними є ті, які прикріплені до стінки судини і рухаються в просвіті. Вони можуть відірватися і з потоком крові переміститися в легеневу артерію.
Гемодинамічні наслідки тромбозу проявляються при ураженні понад 30-50% обсягу легеневого русла. Емболізація судин легенів приводить до підвищення опору в судинах малого кола кровообігу, підвищення навантаження на правий шлуночок, формуванню гострої правошлуночкової недостатності. Однак тяжкість ураження судинного русла визначається не тільки і не стільки обсягом тромбозу артерій, скільки гіперактивацією нейрогуморальних систем, підвищеним викидом серотоніну, тромбоксану, гістаміну, що призводить до вазоконстрикції (звуження просвіту кровоносних судин) і різкого підвищення тиску в легеневій артерії. Страждає перенесення кисню, з’являється гіперкапнія (збільшується рівень вмісту вуглекислого газу в крові). Правий шлуночок розширюється, виникає трикуспідальна недостатність, порушення коронарного кровотоку. Знижується серцевий викид, що приводить до зменшення наповнення лівого шлуночка з розвитком його діастолічної дисфункції. Розвиваючись при цьому системна гіпотензія (зниження артеріального тиску) може супроводжуватися непритомністю, колапсом, кардіогенним шоком, аж до клінічної смерті.
Можлива тимчасова стабілізація артеріального тиску створює ілюзію гемодинамічної стабільності пацієнта. Однак через 24-48 годин розвивається друга хвиля падіння артеріального тиску, причиною якої є повторні тромбоемболії, тромбоз внаслідок недостатньої антикоагулянтної терапії. Системна гіпоксія і недостатність коронарної перфузії (проходження крові) зумовлюють виникнення порочного кола, що приводить до прогресування правошлуночкової недостатності кровообігу.
Емболи невеликого розміру погіршують загальний стан, можуть проявлятися кровохарканням, обмеженими інфаркт-пневмоніями.
Класифікація та стадії розвитку тромбоемболії легеневої артерії
Існує кілька класифікацій ТЕЛА: по гостроті процесу, за обсягом ураженого русла і по швидкості розвитку, але всі вони складні при клінічному застосуванні.
За обсягом ураженого судинного русла розрізняють наступні види ТЕЛА:
- Масивна – емболії локалізується в основному стовбурі або головних гілках легеневої артерії; уражається 50-75% русла. Стан хворого – вкрай важкий, спостерігається тахікардія і зниження артеріального тиску. Відбувається розвиток кардіогенного шоку, гострої правошлуночкової недостатності, характеризується високою летальністю.
- Емболія пайових або сегментарних гілок легеневої артерії – 25-50% ураженого русла. Є всі симптоми захворювання, але артеріальний тиск не знижений.
- Емболія дрібних гілок легеневої артерії – до 25% ураженого русла. У більшості випадків буває двосторонньою і, найчастіше, малосимптомною, а також повторною або рецидивуючою.
Клінічний перебіг ТЕЛА буває гострим ( «блискавичним»), гострим, підгострим (затяжним) і хронічним рецидивуючим. Як правило, швидкість течії захворювання пов’язане з об’ємом тромбування гілок легеневих артерій.
За ступенем тяжкості виділяють важку (реєструється у 16-35%), середньотяжку (у 45-57%) і легку форму (у 15-27%) розвитку захворювання.
Більше значення для визначення прогнозу хворих з ТЕЛА має стратифікація ризику за сучасними шкалами (PESI, sPESI), що включає 11 клінічних показників. На підставі цього індексу пацієнт відноситься до одного з п’яти класів (I-V), в яких 30-денна летальність варіює від 1 до 25%.
Ускладнення тромбоемболії легеневої артерії
Гостра ТЕЛА може служити причиною зупинки серця і раптової смерті. При поступовому розвитку виникає хронічна тромбоемболічна легенева гіпертензія, прогресуюча правошлуночкова недостатність кровообігу.
Хронічна тромбоемболічна легенева гіпертензія (ХТЕЛГ) – форма захворювання, при якій відбувається тромботична обструкція дрібних і середніх гілок легеневої артерії, внаслідок чого підвищується тиск в легеневій артерії і збільшується навантаження на праві відділи серця (передсердя і шлуночок). ХТЕЛГ – унікальна форма захворювання, тому що може бути потенційно виліковна хірургічними і терапевтичними методами. Діагноз встановлюється на підставі даних катетеризації легеневої артерії: підвищення тиску в легеневій артерії вище 25 мм рт. ст., підвищення легеневого судинного опору вище 2 ОД Вуда, виявлення емболів в легеневих артеріях на тлі тривалої антикоагулянтної терапії більше 3-5 місяців.
Важким ускладненням ХТЕЛГ є прогресуюча правошлуночкова недостатність кровообігу. Характерним є слабкість, серцебиття, зниження переносимості навантажень, поява набряків на нижніх кінцівках, накопичення рідини в черевній порожнині (асцит), грудній клітці (гідроторакс), серцевій сумці (гідроперикард). При цьому задишка в горизонтальному положенні відсутня, застою крові в легенях немає. Часто саме з такими симптомами пацієнт вперше потрапляє до кардіолога. Дані про інші причини хвороби відсутні. Тривала декомпенсація кровообігу викликає дистрофію внутрішніх органів, білкове голодування, зниження маси тіла. Прогноз найчастіше несприятливий, можлива тимчасова стабілізація стану на тлі медикаментозної терапії, але резерви серця швидко вичерпуються, набряки прогресують, тривалість життя рідко перевищує 2 роки.
Діагностика тромбоемболії легеневої артерії
Методи діагностики, що застосовуються до конкретних хворих, залежать перш за все від визначення ймовірності ТЕЛА, тяжкості стану пацієнта і можливостей лікувальних установ.
Діагностичний алгоритм представлений в дослідженні PIOPED II (the Prospective Investigation of Pulmonary Embolism Diagnosis) 2014 року.
На першому місці по своїй діагностичній значущості знаходиться Електрокардіографія, яка повинна виконуватися всім пацієнтам. Патологічні зміни на ЕКГ – гостро виникле перевантаження правого передсердя і шлуночка, складні порушення ритму, ознаки недостатності коронарного кровотоку – дозволяють запідозрити захворювання і вибрати правильну тактику, визначаючи тяжкість прогнозу.
Оцінка розмірів і функції правого шлуночка, ступеня трикуспідальної недостатності по ЕхоКГ дозволяє отримати важливу інформацію про стан кровотоку, тиску в легеневій артерії, виключає інші причини важкого стану пацієнта, такі як тампонада перикарда, діссекцію (розсічення) аорти та інші. Однак це не завжди здійснимо в зв’язку з вузьким ультразвуковим вікном, ожирінням пацієнта, неможливістю організувати цілодобову службу УЗД.
Метод визначення D-димеру довів свою високу значимість при підозрі на ТЕЛА. Однак тест не є абсолютно специфічним, так як підвищені результати зустрічаються і при відсутності тромбозу, наприклад, у вагітних, літніх людей, при фібриляції передсердь, злоякісних новоутвореннях. Тому пацієнтам з високою ймовірністю захворювання це дослідження не показано. Однак при низькій вірогідності тест досить інформативний для виключення тромбоутворення в судинному руслі.
Для визначення тромбозу глибоких вен високу чутливість і специфічність має УЗД вен нижніх кінцівок, яке для скринінгу може проводитися в чотирьох точках: пахових і підколінних областях з обох сторін. Збільшення зони дослідження підвищує діагностичну цінність методу.
Комп’ютерна томографія грудної клітини з контрастуванням судин – високодоказовий метод діагностики тромбоемболії легеневої артерії. Дозволяє візуалізувати як великі, так і дрібні гілки легеневої артерії.
При неможливості виконання КТ грудної клітини (вагітність, непереносимість йодовмісних контрастних речовин і т.д.) можливе виконання планарної вентиляційно-перфузійної (V / Q) сцинтиграфії легенів.Цей метод може бути рекомендований багатьом категоріям хворих, однак на сьогоднішній день він залишається малодоступним.
Зондування правих відділів серця і ангіопульмонографія є найбільш інформативними в даний час методом. З його допомогою можна точно визначити як факт емболії, так і обсяг поразки.
На жаль, не всі клініки оснащені ізотопними і ангіографічними лабораторіями. Але виконання скринінгових методик при первинному зверненні пацієнта – ЕКГ, оглядова рентгенографія грудної клітини, УЗД серця, УЗДГ вен нижніх кінцівок – дозволяє направити хворого на МСКТ (мультиспіральну комп’ютерну томографію) і подальше обстеження.
Лікування тромбоемболії легеневої артерії
Основна мета лікування при тромбоемболії легеневої артерії – збереження життя хворого і профілактика формування хронічної легеневої гіпертензії. В першу чергу для цього необхідно зупинити процес тромбоутворення в легеневій артерії, який, як уже говорилося вище, відбувається не одномоментно, а протягом кількох годин або днів.
При масивному тромбозі показано відновлення прохідності закупорених артерій – тромбектомія, так як це призводить до нормалізації гемодинаміки.
Для визначення стратегії лікування використовують шкали визначення ризику смерті в ранній період PESI, sPESI. Вони дозволяють виділити групи хворих, яким показана амбулаторна допомога або необхідна госпіталізація в стаціонар з виконанням МСКТ, екстреній тромботичній терапії, хірургічної тромбектоміі або черезшкірного внутрішньосудинного втручання.
| Параметри | Оригінальний PESI | Спрощений sPESI |
| Вік, років | Вік в роках | 1 (якщо> 80 років) |
| Чоловіча стать | +10 | – |
| Злоякісні новоутворення | +30 | 1 |
| Хронічна серцева недостатність | +10 | 1 |
| Хронічні захворювання легень | +10 | – |
| ЧСС ≥ 110 в хвилину | +20 | 1 |
| Систолічний АТ <110 мм рт. ст. | +30 | 1 |
| Частота дихання> 30 за хвилину | +20 | – |
| Температура <36 ° C (96,8 ° F) | +20 | – |
| Порушення свідомості | +60 | – |
| Сатурація кисню <90% | +20 | 1 |
| Рівні ризику 30-денної летальності | ||
|
Клас I (≤ 65 балів) Дуже низький 0-1,6% |
0 балів – ризик 1% (довірчий інтервал 0-2,1%) |
|
|
Клас II (66-85 балів) Низький ризик 1,7-3,5% |
||
|
Клас III (86-105 балів) Помірний ризик 3,2-7,1% |
≥ 1 балу – ризик 10,9% (довірчий інтервал 8,5-13,2%) |
|
|
Клас IV (106-125 балів) Високий ризик 4, 0-11,4% |
||
|
Клас V (> 126 балів) Дуже високий ризик 10,0-24,5% |
||
| Примітка: ЧСС – частота серцевих скорочень, АТ – артеріальний тиск. | ||
Для поліпшення насосної функції правого шлуночка призначають добутамін (допмін), периферичні вазодилятатори, що зменшують навантаження на серце. Їх краще вводити інгаляційно.
Тромболітична терапія надає свій ефект у 92% хворих, що проявляється поліпшенням основних гемодинамічних показників. Оскільки вона радикально покращує прогноз захворювання, протипоказань до неї менше, ніж при гострому інфаркті міокарда. Однак тромболізис доцільно проводити протягом двох діб після початку тромбозу, в подальшому його ефективність знижується, а геморагічні ускладнення залишаються на колишньому рівні. Пацієнтам низького ризику тромболізис не показаний.
Імплантація венозних фільтрів проводиться у випадках неможливості призначення антикоагулянтів, а також неефективності звичайних доз цих препаратів. Імплантація фільтра, вловлює тромби з периферичних вен, проводиться в нижню порожнисту вену на рівні впадання в неї ниркових вен, в деяких випадках – вище.
У пацієнтів з протипоказаннями до системного фібринолізу може бути застосована методика чрезкатеторної фрагментації тромбу з подальшою аспірацією (вентиляцією) вмісту. Пацієнтам з центральними тромбами в легеневій артерії рекомендується хірургічна емболектомія в разі рефрактерного кардіогенного шоку до терапії, що проводиться, при наявності протипоказань до фібринолітичної терапії або її неефективності.
Кава-фільтр вільно пропускає кров, але вловлює тромби в легеневій артерії.
Тривалість антикоагулянтної терапії у хворих з гострим венозним тромбозом становить не менше трьох місяців. Лікування повинно починатися з внутрішньовенного введення нефракціонованого гепарину до збільшення активованого часткового тромбопластинового часу в 1,5-2 рази в порівнянні з вихідними значеннями. При стабілізації стану можливий перехід на підшкірні ін’єкції низькомолекулярного гепарину з одночасним призначенням варфарину до досягнення цільового МНВ (міжнародного нормалізованого відношення), рівного 2,0-3,0. В даний час більш часто використовуються нові оральні антикоагулянти (прадакса, Ксарелто, еліквіс), серед яких найкращим є Ксарелто (ривароксабан) в зв’язку зі зручним одноразовим прийомом, доведеною ефективністю у найбільш важких груп хворих, відсутністю необхідності контролювати МНВ. Вихідна доза ривароксабана становить 15 мг 2 рази на день протягом 21 дня з переходом на підтримуючу дозу 20 мг.
У ряді випадків антикоагулянтна терапія проводиться більше трьох місяців, іноді – невизначено довго. До таких випадків відносяться пацієнти з повторними епізодами тромбоемболії, тромбозом проксимальних вен, дисфункцією правого шлуночка, антифосфоліпідним синдромом, вовчаковим антикоагуянтом. При цьому нові оральні антикоагулянти ефективніше і безпечніше антагоністів вітаміну К.
Вагітність
Частота ТЕЛА у вагітних варіює від 0,3 до 1 випадку на 1000 пологів. Діагностика складна, так як скарги на задишку можуть бути пов’язані з фізіологічними змінами в організмі жінки. Іонізуюче опромінення протипоказане у зв’язку з його негативним впливом на плід, а рівень D-димера може бути підвищеним у 50% здорових вагітних. Нормальний рівень D-димера дозволяє виключити тромбоемболію легеневої артерії, при підвищенні – направити на додаткові дослідження: УЗД вен нижніх кінцівок. Позитивні результати дослідження дозволяють без проведення рентгенографії грудної клітини призначити антикоагулянти, при негативних результатах показані КТ грудної клітини або перфузійні сцинтиграфія легенів.
Для лікування ТЕЛА у вагітних використовуються низькомолекулярні гепарини. Вони не проникають через плаценту, не викликають порушення розвитку плоду. Їх призначають тривалим курсом (до трьох місяців), аж до пологів. Антагоністи вітаміну К проникають через плаценту, викликаючи вади розвитку при призначенні в першому триместрі і кровотечі у плода в третьому триместрі вагітності. Можливо обережне застосування в другому триместрі вагітності (по аналогії з веденням жінок з механічними протезами клапанів серця). Нові оральні антикоагулянти вагітним протипоказані.
Антикоагулянтну терапію слід продовжувати три місяці після пологів. Тут можна застосовувати варфарин, так як він не проникає в грудне молоко.
Прогноз. Профілактика
Запобігти розвитку ТЕЛА можна, усунувши або максимально знизивши ризик тромбоутворення. Для цього використовують всі можливі методи:
- максимальне скорочення тривалості постільного режиму при знаходженні в стаціонарі при будь-яких захворюваннях;
- еластична компресія нижніх кінцівок спеціальними бинтами, панчохами при наявності варикозної хвороби.
Крім того людям з групи ризику в плановому порядку призначають антикоагулянти для профілактики утворення тромбів. До такої групи ризику відносяться:
- люди, старше 40 років;
- пацієнти, які страждають злоякісними пухлинами;
- лежачі хворі;
- люди, що раніше перенесли епізоди тромбозу в післяопераційному періоді після хірургічного втручання на колінному, тазостегновому суглобі і ін.
Протиемболічні панчохи рекомендуються при більшості хірургічних втручань, що вимагають іммобілізації (знаходження в стані спокою).
При тривалих перельотах необхідно забезпечити питний режим, вставати і ходити кожні 1,5 години, перед перельотом прийняти 1 таблетку аспірину, навіть якщо пацієнт не приймає аспірин для профілактики постійно.
При вже наявному венозному тромбозі може бути проведена і хірургічна профілактика методами:
- імплантації фільтра в нижню порожнисту вену;
- ендоваскулярної катетерної тромбектомії (видалення тромбу з вени за допомогою введеного в нього катетера);
- перев’язки великої підшкірної або стегнової вен – основних джерел тромбів.

Головний видавець і засновник сайту healthapple.info з 31 травня 2017 року. Редактор статей на сайті.